アセトアニリド ニトロ化 オルト 183070-アセトアニリド ニトロ化 オルト
ニトロアセトアニリドに関するQ&Aの一覧ページです。 オルト体がほとんど生成しない理由を説明せよ。 教科書を見てもいまいち分かりません。 アニリンを直接ニトロ化することなく、アミノ基を保護してアセトアニリドにしてから混酸を加えてアセトアニリド ニトロ化 温度 15 By November 18, November 18, News > 教授には続きを読む, ニトロフェノールのオルト体とパラ体では沸点が相当違いますよねぇ・・・。 ニトロ基の場所の違いがどうして沸点の差に結びつくんでしょう? 沸騰するってこの実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。
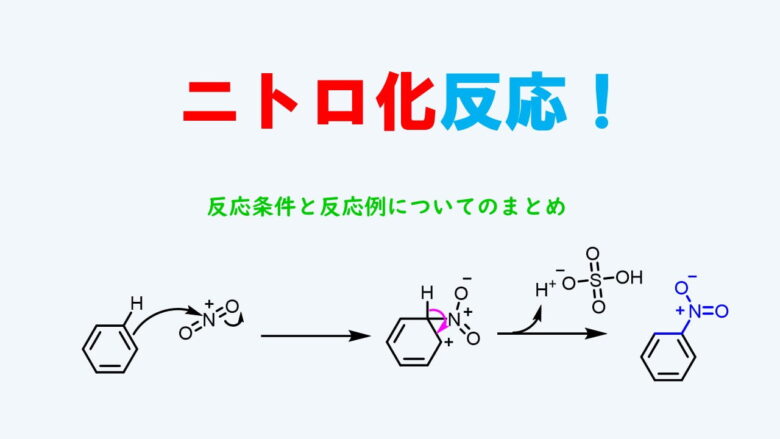
ニトロ化反応の条件とやり方 ネットdeカガク
アセトアニリド ニトロ化 オルト
アセトアニリド ニトロ化 オルト-なおアセトアニリドの場合、nhcoch 3 という置換基が存在します。それなりに大きな置換基なので、立体障害は大きくなります。そのためオルトよりも、パラの位置で求電子置換反応を起こす可能性が高くなります。 芳香族求電子置換反応を理解するこの反応は、一般的に「ニトロ化 (nitration) 」と呼ばれます。 図13 ベンゼンのニトロ化 (iv) スルホン化 スルホ基 (SO 3 H) を芳香環に導入するためには、濃硫酸 H 2 SO 4 あるいは濃硫酸に過剰の三酸化硫黄 SO 3 を吸収させた発煙硫酸が使用されます。



ナフトールの配向性 Okwave
–45– 312 アセトアニリドのニトロ化 10乾燥させた50 mLのビーカーに1)で得たアセトアニリド11をすべて入れ、濃硫酸12を加え てよくかき混ぜ2、アセトアニリドを溶解する。アセトアニリドが溶けたら、ビーカーの氷水浴に子育てと学校 > 大学、短大、大学院 > 大学 アセトアニリドをニトロ化した時の生成物はほとんどがパラ体 (pニトロアセトアニリド)である。 オ オルト体がほとんど生成しない理由を説明せよ。 教科書を見てもいまいち分かりません。 どなたか教えてなおアセトアニリドの場合、nhcoch 3 という置換基が存在します。それなりに大きな置換基なので、立体障害は大きくなります。そのためオルトよりも、パラの位置で求電子置換反応を起こす可能性が高くなります。 芳香族求電子置換反応を理解する
5.3-ニトロアセトフェノンを効率よく合成するには、ベンゼンをニトロ化後アセチル化する方法1よりも、アセチル化後ニトロ化する方法2のほうが良い。, ・芳香族に結合している置換基が電子供与性の場合、オルト、パラ配向性 "Lanthanide triflate and triflide実験テーマB 芳香族化合物は、ニトロ化、スルフォン化、ハロゲン化等の求電子置換反応を受ける。 置換基を有するベンゼン誘導体は、試薬の反応する位置の違いによって、異性体を生ずる可能性がある。 この実験では、アセトアニリドのニトロ化反応をアセトアニリドのニトロ化(hno3, h2so4)は、オルト位(痕跡)、パラ位(90%)です。この実験事実からも立体障害が大きな理由で有ると考えます。 更に、pニトロ体をニトロ化してもオルト位のニトロ化は反応条件を強くしないかぎりおきないのです。 一方のオルト位のみにアルキル基をもっape
この反応は、一般的に「ニトロ化 (nitration) 」と呼ばれます。 図13 ベンゼンのニトロ化 (iv) スルホン化 スルホ基 (SO 3 H) を芳香環に導入するためには、濃硫酸 H 2 SO 4 あるいは濃硫酸に過剰の三酸化硫黄 SO 3 を吸収させた発煙硫酸が使用されます。今日の実験はアセトアニリドを濃硫酸触媒下で濃硝酸と反応させ、 ニトロアセトアニリドのパラ体を合成する実験をやった。 ただし、オルト体のものも生成するため、 途中で分離作業を要する。 手順は主に、 ニトロ化反応 1:ナスフラスコにアセトアニリドを500g程度定量し、濃硫酸11mlアセトアニリドのニトロ化では、アセチルアミノ基のかさ高さが、立体障害となって、オルト位に入りにくいのではないでしょうか。 オルトに対し、隣の隣(1位と3位)をメタ (meta , m) 、反対側(1位と4位)をパラ (para , p) という。
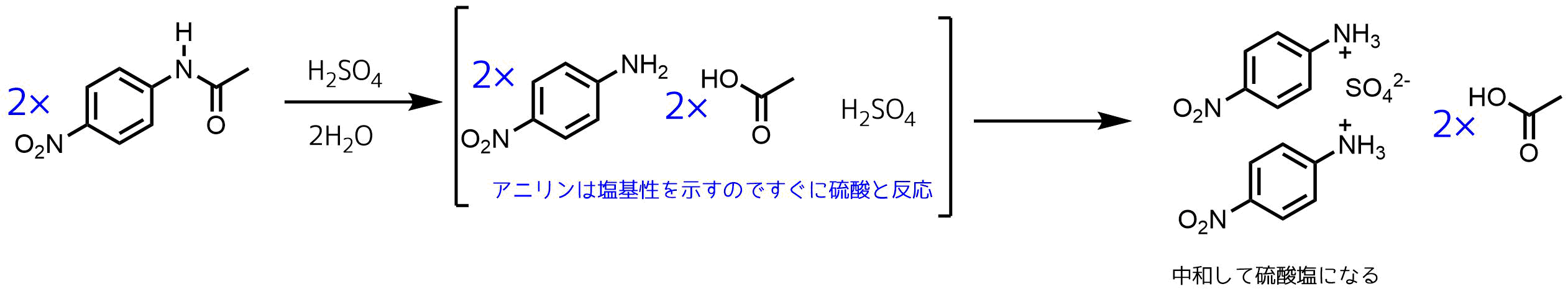


ニトロ化反応の条件とやり方 ネットdeカガク


有機反応機構 芳香族求電子置換反応
Mニトロアセトアニリド97 (3)396 (3)396 不純物または安定化添加剤非該当 4 応急措置 吸入した場合 新鮮な空気のある場所に移すこと。 症状が続く場合には、医師に連絡すること。 皮膚に付着した場合 すぐに石鹸と大量の水で洗浄すること。アセトアニリドはオルトメタ配向性ということなので、 ニトロ化すると生成物のほとんどがoニトロアセトアニリドとpニトロアセトアニリドだと思うのですが、 oニトロアセトアニリドよりもpニトロアセトアニリドのほうが多く生成される理由は、 分子2)はベンゼンへのニトロ化反応で、オルト、メタ、パラ配向の区別は無い(問題14参照)。 OCH2CH3 HNO3 H2SO4 1) HNO3 H2SO4 2) Cl HNO3 H2SO4 3) HNO3 H2SO4 4) NO2 NOH O O HNO3 nitric acid (base) OS O O HOH H2SO4 sulfuric acid (acid) NO OH H S O OH O H2O ONO nitronium ion (1) (2) ONO H N HO O


有機化学についての質問です 下の図のn N Dimethylanilineを Yahoo 知恵袋
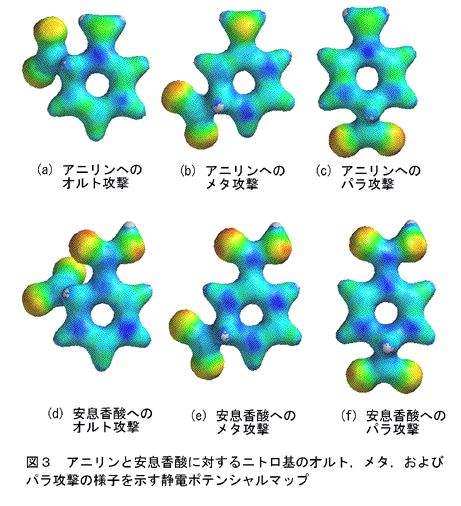


有機化学第一教室
実験実施日 1999年6月17日(木) 曇り 気温:28℃ 湿度:% 気圧:1006hPa 実験時間:13:00~17:00 実験テーマ;ニトロ化が有名なのは、芳香族化合物の基本的な反応であること、ニトロ基が他の官能基に変換しやすいことが理由です。 アミドなどの置換基に対してオルト pニトロアセトアニリドの酸加水分解の反応機構については一般化すると酸アミド実験実施日 1999年6月17日(木) 曇り 気温:28℃ 湿度:% 気圧:1006hPa 実験時間:13:00~17:00 実験テーマ;
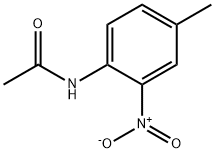


4 Methyl 2 Nitroacetanilide Cas 612 45 3



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ
アセトアニリド 求電子置換反応(ニトロ化)の配向性・反応性 95回薬剤師国家試験問10b 第95回薬剤師国家試験 問10b 芳香族化合物に関する記述の正誤を判定してみよう。 b アセトアニリドヘの求電子的ニトロ化反応は、メタ位に比べ、オルト位及びパラ位この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー(TLC) で oニ トロアニリンが副生したことを確認する。下記カテゴリー内の "50 アセトアニリド ニトロ化"に関連する他の関連記事を探す #アセトアニリド ニトロ化 #アセトアニリド ニトロ化 オルト #アセトアニリド ニトロ化 温度 #アセトアニリド ニトロ化 硝酸 #アセトアニリド ニトロ化 酢酸



ニトロ化反応の条件とやり方 ネットdeカガク



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ
今日の実験はアセトアニリドを濃硫酸触媒下で濃硝酸と反応させ、 ニトロアセトアニリドのパラ体を合成する実験をやった。 ただし、オルト体のものも生成するため、 途中で分離作業を要する。 手順は主に、 ニトロ化反応 1:ナスフラスコにアセトアニリドを500g程度定量し、濃硫酸11ml下記カテゴリー内の "50 アセトアニリド ニトロ化"に関連する他の関連記事を探す #アセトアニリド ニトロ化 #アセトアニリド ニトロ化 オルト #アセトアニリド ニトロ化 温度 #アセトアニリド ニトロ化 硝酸 #アセトアニリド ニトロ化 酢酸アセトアニリドのニトロ化では、アセチルアミノ基のかさ高さが、立体障害となって、オルト位に入りにくいのではないでしょうか。 オルトに対し、隣の隣(1位と3位)をメタ (meta , m) 、反対側(1位と4位)をパラ (para , p) という。


放課後化学講義室 オルト メタ パラ そしてイプソ



アニリンのニトロ化の生成過程 反応中間体の共鳴式 アニリンをニトロ 化学 教えて Goo
アニリンのアセチル化の実験を通じて、試薬の調合、吸引沪過、再結晶など、有機化合物の合 成に必要な基本操作を習得する。 2 反応式 ch3c o o cch3 o h n cch3 o ho cch3 o アニリン 無水酢酸 アセトアニリド 酢酸 c c c c c c n c o o c o h h h h h h c h h c h h h h c c c c cアセトアニリドのニトロ化では、アセチルアミノ基のかさ高さが、立体障害となって、オルト位に入りにくいのではないでしょうか。 オルトに対し、隣の隣(1位と3位)をメタ (meta , m) 、反対側(1位と4位)をパラ (para , p) という。この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー(TLC) で oニ トロアニリンが副生したことを確認する。
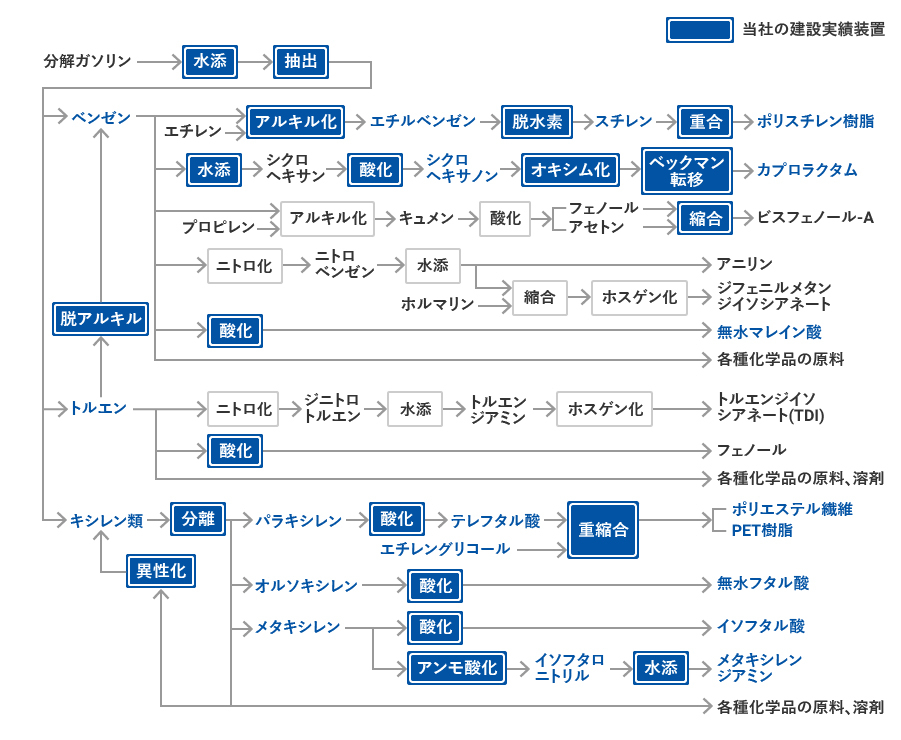


芳香族系誘導品 千代田化工建設株式会社
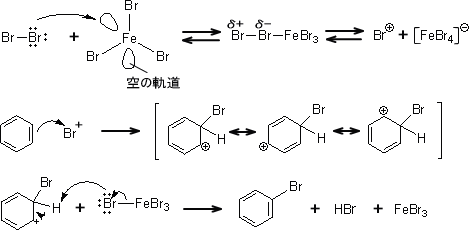


芳香族化合物の反応性


ここに フェノールのニトロ化はオルト パラ配向性であると書かれ Yahoo 知恵袋
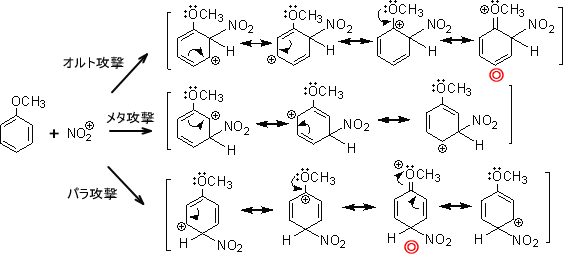


芳香族化合物の反応性



P ニトロアセトアニリドのさらなるニトロ化 Okwave
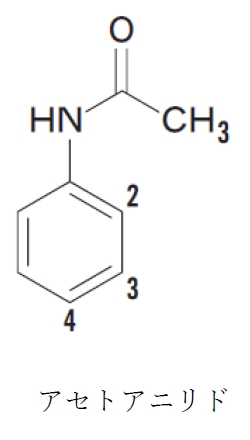


アセトアニリド 求電子置換反応 ニトロ化 の配向性 反応性 95回問10b
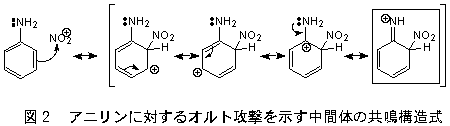


有機化学第一教室



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ



P ニトロベンゼンのモノニトロ化配向性 Okwave


アセトアニリドをニトロ化する際 固体のアセトアニリドに濃硫酸 Yahoo 知恵袋


有機反応機構 芳香族求電子置換反応



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学


有機反応機構 芳香族求電子置換反応



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学



アニリン版クメン法 Chem Station ケムステ
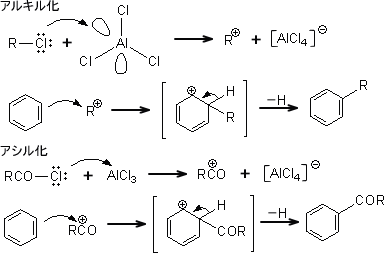


芳香族化合物の反応性
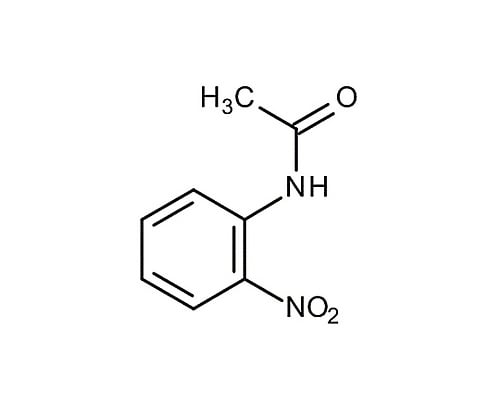


61 0365 02 2 ニトロアセトアニリド 合成用 0879 100g 8 879 0100 Axel アズワン
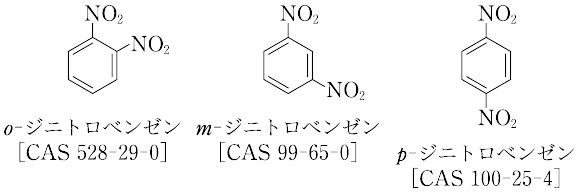


ジニトロベンゼンとは コトバンク
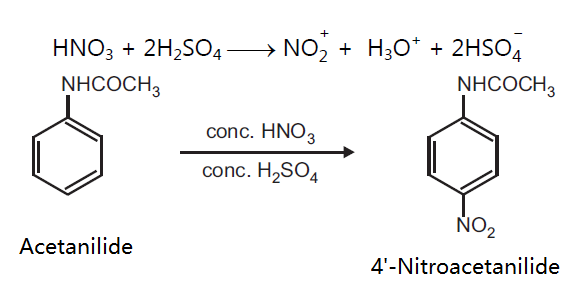


4 ニトロアセトアニリド 104 04 1
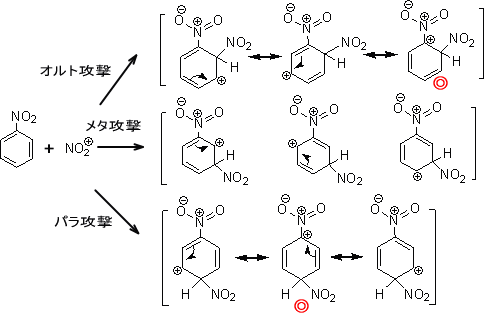


芳香族化合物の反応性


放課後化学講義室 オルト メタ パラ そしてイプソ



ナフトールの配向性 ベンゼンの置換基によってオルト パラ配向性 メ 化学 教えて Goo



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ


環化 問6
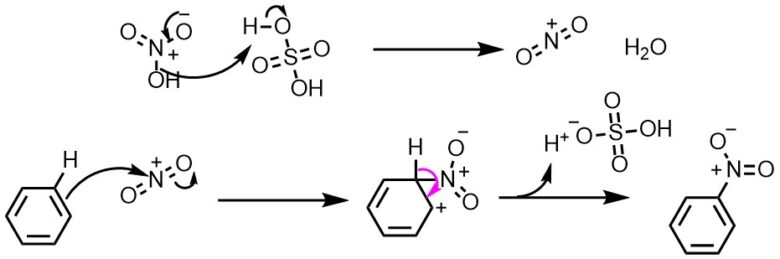


ニトロ化反応の条件とやり方 ネットdeカガク
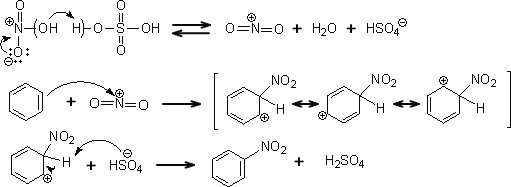


芳香族化合物の反応性



ニトロベンゼンからアニリンを合成する語呂合わせなど 17h29大学入学共通テスト試行調査第1回第3問 問4 入試化学を語呂合わせで解く大学入試ゴロ化学


マクマリーの16 35 Dの問題でnnジエチルアニリンをスルホ Yahoo 知恵袋
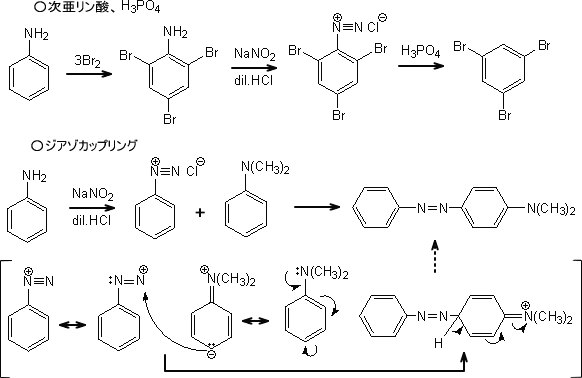


芳香族化合物の反応性
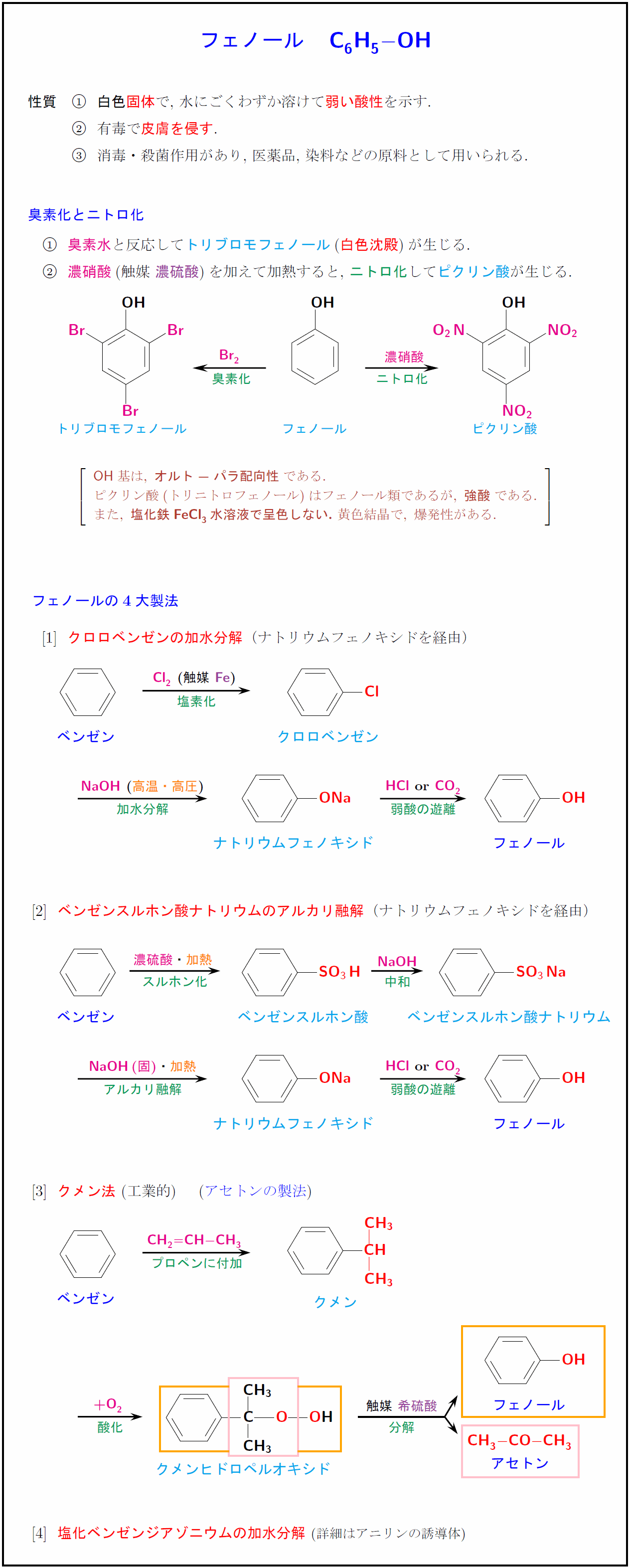


高校有機化学 フェノール C H Oh の性質 臭素化とニトロ化 4大製法まとめ 受験の月


オルト体 に関するq A Yahoo 知恵袋
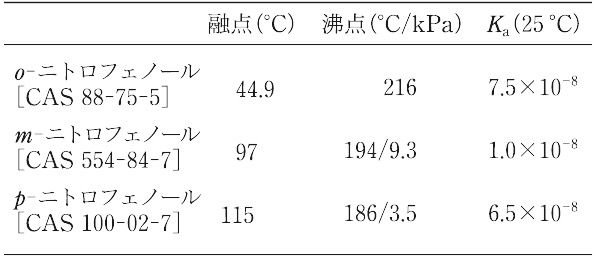


ニトロフェノールとは コトバンク
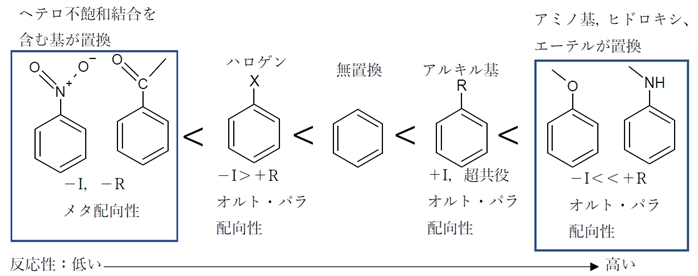


アセトアニリド 求電子置換反応 ニトロ化 の配向性 反応性 95回問10b


エヌアセチルオルトトルイジンをニトロ化すると何ができるのか教えて Yahoo 知恵袋



4 ニトロアニリン Wikipedia


ハメット則


環化 問6


環化 問6
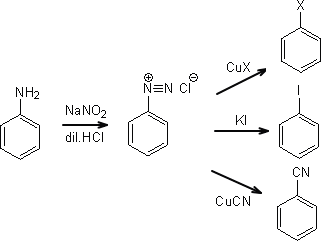


芳香族化合物の反応性
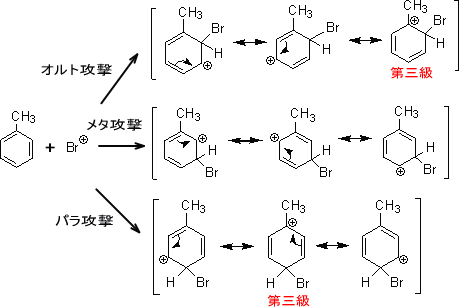


芳香族化合物の反応性
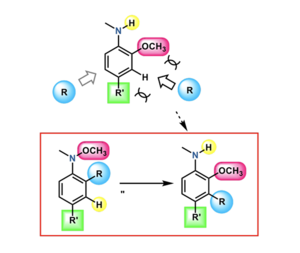


ドミノ転位反応で新規アニリンの効率的な合成法を開発 新薬 新材料開発への応用を期待 お知らせ 東北大学大学院理学研究科 理学部


2 3 4 反応性 配向性に及ぼす置換基の効果 Yaku Tik 薬学まとめました
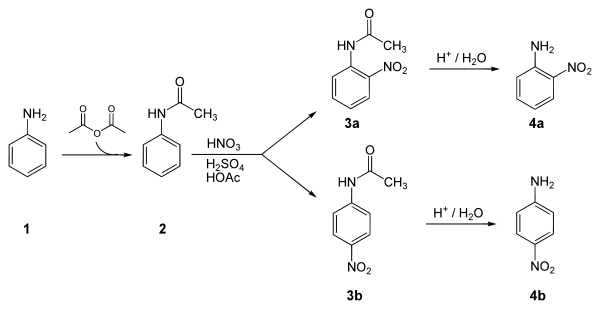


4 ニトロアニリン Wikipedia



Sandmeyer反応はアニリンを起点とする官能基導入法 とらおの有機化学



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学



Pcゲーマーな薬学生の奮闘記 有機化学


ほんとは簡単 ジアゾ化 カップリングを解説 受験メモ


有機反応機構 芳香族求電子置換反応



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ


Research A Of Organofluorochemlab


放課後化学講義室 オルト メタ パラ そしてイプソ


有機反応機構 芳香族求電子置換反応



ナフトールの配向性 Okwave
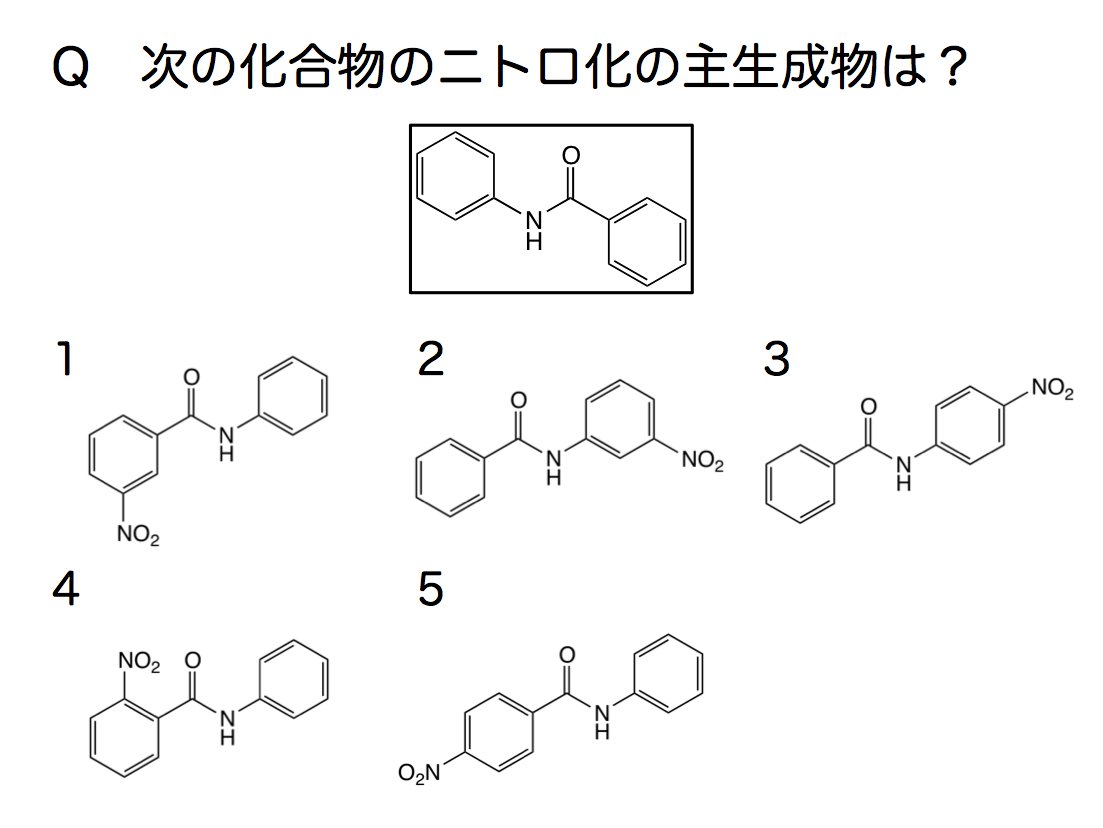


アセトアニリド ニトロ化 人気のある画像を投稿する



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ


ほんとは簡単 ジアゾ化 カップリングを解説 受験メモ
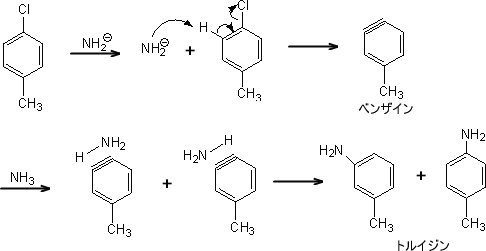


芳香族化合物の反応性


有機化学の質問です ベンゼンを起点にm ブロモクロロベンゼンを合成する Yahoo 知恵袋


ニトロアニリン 4
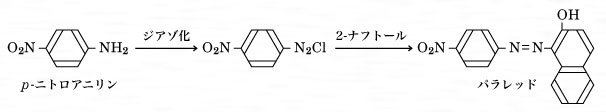


ニトロアニリンとは コトバンク



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学


有機反応機構 芳香族求電子置換反応


放課後化学講義室 オルト メタ パラ そしてイプソ



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学
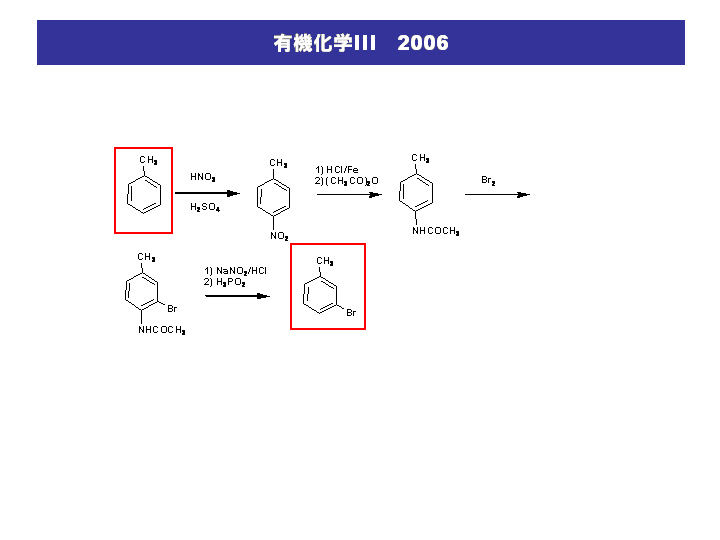


神大工応化 有機化学iii



アニリンのニトロ化 アニリンをニトロ化する際 直接ニトロ化するので 化学 教えて Goo
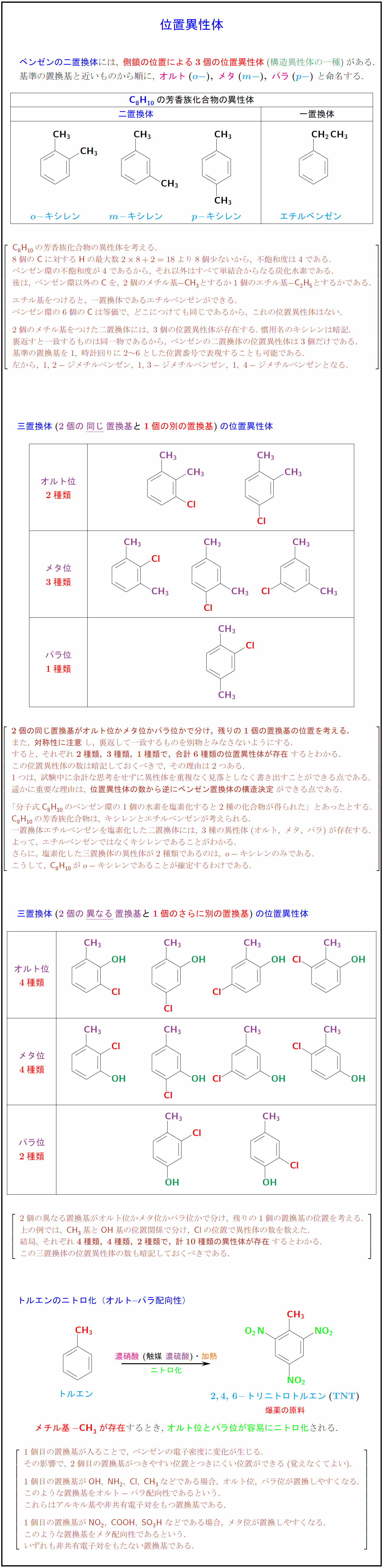


高校有機化学 位置異性体 ベンゼンの置換体 とトルエンのニトロ化 受験の月


環化 問6


有機反応機構 芳香族求電子置換反応



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学



2 ニトロアニリン Wikipedia
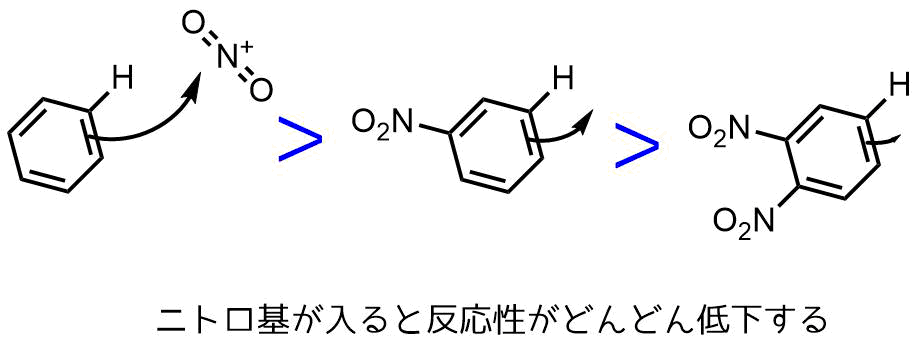


ニトロ化反応の条件とやり方 ネットdeカガク



コメント
コメントを投稿